 流行病学
流行病学
流行病学:门静脉血栓形成的发生率文献报道差别很大。Jones报道
肝硬化门静脉系统血栓的发生率为10%,Okuda报道日本病理协会247728例患者的尸解结果,门静脉栓塞的发生率为0.5489%,
肝硬化患者门静脉栓塞率为6.5885%,脾切除术后门静脉栓塞率为22.2%。Egnchi报道特发性门静脉高压症脾切除术后门静脉栓塞率为25%。Rattner等调查1000例脾切除术,7例发生了门静脉栓塞,发生率为0.7%。Chaffanjon报告了连续60例脾切除的病人,术后常规应用低分子肝素,每天3000U皮下注射,术前及术后7天、30天,采用彩色多普勒超声检查,发现术后门
静脉血栓发生率为8.3%,其中75%的患者无明显的临床表现。应嘉均等施行脾切除2185例,术后5例出现PT,发生率0.23%。Rosemurgy报告门腔静脉架桥分流术后栓塞率为10%。戴植本报告24例门静脉高压症离断术后患者,术前门静脉栓塞率8.33%,术后栓塞率为37.5%,而TIPS术后的栓塞率高达32.5%。单纯肠系膜
静脉血栓的发生率则占住院患者的0.002%~0.007%,占全部肠系膜栓塞病例的10%。另外调查的41例肝外型门静脉高压症的患者中,门静脉血栓形成33例,先天性肠系膜多发性动静脉瘘2例,先天性多发性肝动脉细小分支-门静脉瘘1例,后天性肝总动脉-脾静脉瘘1例,脾动-静脉瘘1例,终末支门静脉纤维化2例,肝动脉瘤压迫门静脉致
血栓形成且瘤体远端
血栓形成1例,其中4例因门静脉血栓形成而并发急性
肠系膜静脉血栓形成。又有文献报道门
静脉血栓在肝移植的术前及术后的发生率均有增加,发生率2.1%~13%不等。门
静脉血栓发生的影响因素包括
肝硬化、高凝血状态、脾切除史、门腔分流病史等。
门
静脉血栓的发生与性别、
肝硬化程度、酒精性
肝硬化等因素也有关系。男性比女性发病率高,
肝硬化A级发生率为2.5%,B级为5.6%,C级为10.4%;酒精性
肝硬化发生率为17%,而非酒精性
肝硬化发生率为10%。考虑到不典型病例的漏诊,甚至某些患者死后也未能做出正确诊断,门
静脉血栓的实际发生率比文献报道的还要高。
 病因
病因
病因:门静脉血栓形成的病因很复杂,主要有炎症性、肿瘤性、凝血功能障碍性、腹腔手术后、外伤性及原因不明性等。25%~30%的成人门
静脉血栓病例继发于
肝硬化。婴幼儿门
静脉血栓多继发于先天性门静脉闭锁、脐静脉脓毒血症、阑尾炎等。PT可分为原发性与继发性两种。原发性多与血液高凝状态有关。国外报道372例继发性
肠系膜静脉血栓形成患者,发现周围静脉炎、腹腔炎症性疾病、腹部大手术与门静脉高压是发生的主要因素,且以脾切除术后为常见。局部因素在PT形成的危险因素中占40%,局部因素的存在促进了门
静脉血栓的形成,这些局部因素主要分4类:局部感染灶、门静脉系统损伤、腹腔肿瘤和
肝硬化,临床上以
肝硬化伴发PT为最多。PT还可见于妊娠(特别是子痫患者)、口服避孕药和引起门静脉淤血的患者(如肝静脉阻塞、慢性心力衰竭、
缩窄性心包炎)。有学者认为至少有1/3的PT患者是多种危险因素联合作用的结果。
1.门静脉高压症 多因各种病因的
肝硬化及充血性
脾大所致。主要是由于门静脉压力升高,造成门静脉及其属支的向肝性血流的减少和血流速度的减慢造成涡流而致血小板堆积形成血栓。
2.腹腔感染 为肠道感染性病灶的细菌进入门静脉系统所引起,如新生儿
脐炎、脐静脉脓毒血症,成人常见的有
急性阑尾炎、胰腺炎、胆囊炎、空腔脏器的穿孔、小肠炎性病变、腹腔盆腔脓肿及腹部术后感染等。
3.腹部手术及外伤 各种腹腔的手术均可导致门静脉系统的
血栓形成,特别是脾切除术后最常见。可能与术后血小板增多和血液黏稠度升高有关。脾切除术后门静脉血流量减少,门静脉压力下降加速了血栓的形成。此外,术后扩张的脾静脉内血流缓慢,在高凝状态下又促成了脾
静脉血栓形成。
4.血液处于高凝状态 腹部肿瘤,特别是结肠及胰腺的肿瘤,常伴有门静脉系统的高凝状态,可导致
血栓形成。近年来还发现遗传性凝血功能紊乱也参与门
静脉血栓的形成,包括蛋白C、蛋白S和抗凝血酶缺陷等。
5.肿瘤等压迫门静脉 肿瘤(如胰腺肿瘤、肝细胞癌)压迫、肠扭转等导致门静脉系统血流受阻,致门静脉血栓形成。
6.其他原因 包括原发性小静脉硬化、脾静脉或肠系膜
静脉血栓的蔓延、部分患者有长期服用避孕药史,少见的因素有各种
充血性心力衰竭、红细胞增多症等。
 发病机制
发病机制
发病机制:门静脉阻塞可由PT、恶性肿瘤的侵犯(肝细胞癌栓)等引起,临床上PT是造成门静脉阻塞的主要原因。PT可发生在门静脉主干、肠系膜上静脉、肠系膜下静脉及脾静脉内。如果血栓仅局限于门静脉主干,且为缓慢形成的不完全性阻塞,临床上可能不会发生严重的后果,将来可造成门静脉系统压力升高,血流经胃冠状静脉、食管静脉至半奇静脉,最后注入上腔静脉,由此导致食管胃底静脉曲张。如果门静脉主干和肠系膜上静脉均有
血栓形成,可引起明显后果,严重者可以引起肠坏死,表现为肠壁增厚及肠系膜呈暗红色,黏膜下充血、水肿、出血及肠黏膜剥脱等改变,伴有血性浆液性
腹水,静脉内可挤出新、老血栓。当脾
静脉血栓形成时,脾静脉血流经胃底静脉,最后注入门静脉,进一步加重食管及胃底静脉曲张,甚至破裂出血。单纯肠系膜上静脉和肠系膜下静脉阻塞少见,由于侧支循环丰富,亦较少引起出血,除非血栓原发于
肝硬化者。其他原发因素引起的PT,即使肝外门静脉或肝内较大分支发生阻塞,临床上也很少影响肝脏的结构和功能,偶可致肝坏死,其主要原因是在门静脉血栓形成部位快速建立侧支静脉旁路,最终形成海绵状血管瘤,一定程度上保证了向肝的血流供应。肝内门静脉阻塞,常伴有肝脏结构及功能受损。
 临床表现
临床表现
临床表现:
1.急性型 发病突起,有剧烈
腹痛、
腹胀和呕吐,主要因胃肠淤血所致;若血栓繁衍至肠系膜上静脉,则可有
腹泻、血便、
腹痛、
腹胀、腹部压痛、腹肌紧张和叩击痛等腹膜炎或
麻痹性肠梗阻的表现。在婴幼儿,可表现为突发性
上消化道出血,
脾肿大多属轻微;若血栓蔓延至门静脉主干及肝内分支则可出现大量
腹水。
2.慢性型 病人若渡过急性期,由于门-体静脉建立了广泛的侧支循环――即自然分流的形成,
腹水可能缓解或减少,
脾肿大常是一个突出的症状。一般来说,脾脏肿大的程度取决于病程的长短;脾脏长期充血后,脾髓细胞增生及纤维组织沉积,大量抑血细胞使血细胞破坏增多,出现
脾功能亢进,临床表现为不同程度的贫血、血小板计数减少。此时部分患者发生鼻出血,但很少发生紫癜。
若门
静脉血栓累及门静脉主干和脾静脉,则因门静脉的血流经腰静脉及腹膜后静脉的侧支循环进入体静脉,很少或没有门-奇静脉间的侧支循环,故无食管静脉曲张和出血。值得提出的是小儿对门静脉高压症大出血耐受性好,且由于血管弹性好,腹膜后形成自然分流快而丰富,第1次出血后,若迟至15岁后仍无出血复发,行消化道造影和内镜检查又无发生出血的先兆,手术并非都必须进行。
部分病例可有轻度
黄疸,但肝性脑病少见。其他症状如
腹胀、消化不良、食欲不振等多较轻。
 其他辅助检查
其他辅助检查
其他辅助检查:
1.腹部X线平片 合并肠坏死或麻痹性肠梗阻时,可见肠管扩张增粗伴气液平面。
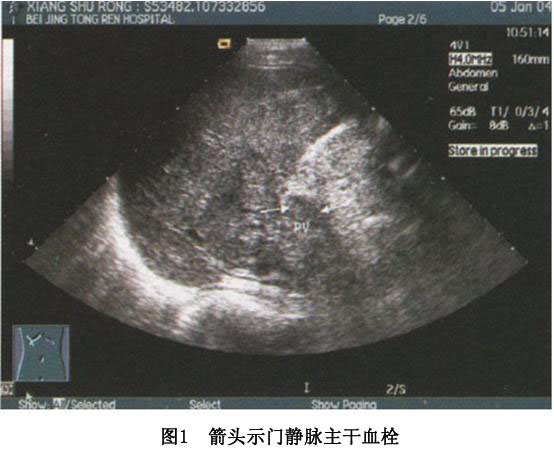
2.腹部B超 显示门静脉血栓形成的部位、大小、范围。主要发现门静脉主干、脾静脉残端内和肠系膜上静脉主干增宽,静脉内有异常回声,为实质性不规则性强光点或等回声光点(图1)。有门静脉海绵样变者,门静脉主干及分支消失,门静脉为小而不规则的管状结构所代替。
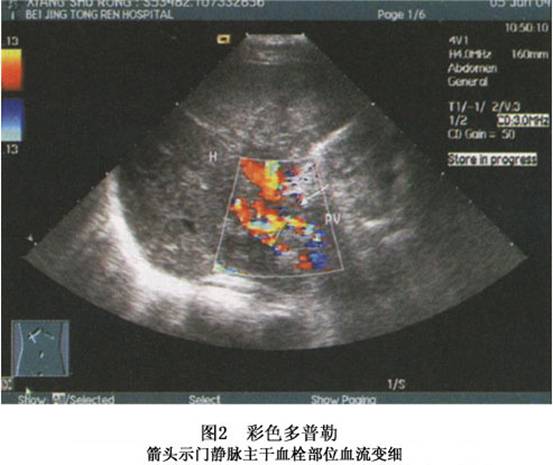
3.彩色多普勒(图2) 门静脉、脾静脉或肠系膜上静脉内径增宽并探及实质性回声,血流变细,完全阻塞时血流信号消失,栓塞远侧静脉扩张。
4.腹部CT 包括常规平扫及增强扫描(动脉期和静脉期)。门静脉血栓的CT典型征象是门静脉腔内出现不强化低密度条状或块状病灶,并可见侧支静脉及异常肠段,正确率超过90%。同时可发现脾大或脾厚。
5.血管造影 直接或间接门静脉造影可显示血栓形成的位置、范围,诊断率为63%~91%。在门静脉或脾静脉血栓形成处显示造影剂的充盈缺损或完全不显影。梗阻远端和脾静脉扩张、迂曲、延长和移位。梗阻近段和肝内门静脉分支不见造影剂充盈。脾脏内有大量造影剂滞留。
6.磁共振血管造影术 对于门静脉系统的评价不仅十分准确,并且可以比超声、CT提供更多的有关侧支循环的信息。可以了解门静脉系统通畅性、血栓形成、曲张静脉、自发性分流等。敏感性和特异性极高。
 鉴别诊断
鉴别诊断
鉴别诊断:
1.急性
肠梗阻 表现为腹部膨隆,
腹痛剧烈呈阵发性加剧,体检可见肠型或逆蠕动波,肠鸣音亢进呈气过水声或金属音调。
麻痹性肠梗阻时,则肠鸣音减弱或消失。腹部X线透视或平片检查可见肠腔内有多个阶梯状液平,少数患者既往有腹部手术史。
2.慢性胆囊炎 疼痛部位多位于右上腹,可放射至右侧背部和肩胛区。疼痛常在进食油腻食物后加重。B超或CT等检查可确立诊断,有时可发现与
胆囊结石并存,而胰腺的形态正常、胰管无扩张表现。但必须指出少数患者慢性胆囊炎、
胆囊结石与慢性胰腺炎可同时存在。
3.慢性胰腺炎 胰腺癌患者临床上所表现的上腹饱胀、隐痛、
腹泻及消瘦等症状并非其特有,慢性胰腺炎患者同样存在上述症状,并且后者也可出现
黄疸和肿块而酷似胰腺癌,故两者鉴别十分困难。但慢性胰腺炎一般病史较长,且有反复发作史,
腹泻和消瘦症状仅在经历较长病程后才显著。胰腺癌病程较短,无反复发作史,消瘦则较早出现。胰腺炎时腹部X线平片可发现胰腺钙化点。B超、CT检查或胰腺肿块组织细胞学检查可确定诊断。必须指出,慢性胰腺炎可演变为胰腺癌。
 治疗
治疗
治疗:门静脉血栓形成的急性型,宜行内科治疗,如抗凝、祛聚、溶栓、解痉,对发生出血的病例,应以止血、抗休克为主。
对慢性病例,总的目标是制止食管、胃底静脉的破裂出血,抢救生命;降低门静脉压力,防止复发出血;解除脾功能亢进。
1.止血措施 针对出血,临床医师很难估计病人将出多少血,采用什么方法能一劳永逸地防治出血复发,因此对发生出血者,即使是小量的呕血或黑便,也应引起重视。首先采用内科疗法,如病人静息卧床、禁食、补充营养、止血剂应用、三腔二囊管压迫(小儿可采用适当型号的Foley导尿管),亦可在食管内镜下向曲张静脉注射硬化剂。后者简便、安全、有效、可反复进行。多数学者不主张紧急手术,倾向于尽量采取保守疗法控制出血,待病情稳定后,再择期做减压术。
2.防治出血的手术 由于门静脉血栓形成时肝功能损害多较轻,因而对分流手术的耐受性较好,效果亦可靠;而断流术的远期效果多不能令人满意,因此对此类病人应首选分流术。在众多的分流术中又如何选择具体的方法呢?以下几个方面供参考:①降压稳妥、持久;②尽量要求符合生理;③留有余地,一旦出血复发,尚有补救措施。以下就几种手术做一简单介绍:
(1)门静脉旁路术:亦称短路分流,即在受阻的门静脉远近端之间架桥或短路吻合,使内脏的静脉血流流入肝内门静脉,从而恢复门静脉血流的正常循环,符合生理。但必须在肝内表浅部位有可供吻合的相应口径的门静脉分支,国内目前尚未见报道。
(2)改良脾、大网膜肺固定术:日本学者Akita通过动物实验证明,肺组织有从邻近淤血的脏器组织中夺取并转运血液的特性,其方式是接触、粘连、侧支血管形成、高压状态的血流被转运、分流。1960年Akita设计、创用脾-肺固定术治疗肝内型门脉高压症和布-加氏综合征获得成功。1983年郑州大学许培钦引进并改良脾、大网膜肺固定术治疗下腔静脉膜性梗阻取得满意效果,至1999年共手术治疗布-加氏综合征及肝内性门静脉高压症202例,取得良好疗效。
(3)肠系膜上静脉-下腔静脉人工血管C形架桥术联合冠状静脉、脾动脉结扎术:本手术亦称“三联术”,于进腹后,经网膜内胰腺上缘结扎脾动脉、冠状静脉和胰胃皱襞中的胃后血管支。若脾脏巨大,可行大部切除。用直径1.0cm带环的人工血管(Gore-Tex)行肠-腔C形架桥。自1990年以来郑州大学第一附属医院及外院会诊共做“三联术”86例,获得满意效果。
3.肠切除术 主要针对肠系膜血栓形成患者有肠坏死时,坏死肠段及肠系膜切除是惟一的治疗方法。术后持续抗凝预防血栓再形成。
综上所述,对门静脉血栓形成及其产生的后果,多需外科治疗,若条件允许,应首选门静脉旁路术,它恢复了门静脉血液的正常循环,但要求肝内必须有可供吻合的门静脉分支,也要求手术医师具备相应的操作技术和所需的人工血管。而改良脾-肺固定术不仅简便、易行、便于推广,且由于门-肺间侧支循环是逐渐增多、增粗,分流量是逐渐增加的,机体内环境有一调节和适应过程,可能是肝性脑病发生率低于传统门体分流术的主要原因之一。脾-肺固定术后,再发出血率不仅很低,且出血量较少。不言而喻,经胸入路,不仅对脾动脉结扎简便易行,且因食管下段和贲门部暴露充分,对贲门周围血管的离断亦能更彻底和规范,这样不仅可以有效防止术后近期出血,且由于阻断了门-奇静脉间的自然分流,减少了离肝血流,对维护肝脏功能也有裨益。脾动脉结扎或脾部分切除,由于保留了脾脏组织,就保留了脾脏功能,特别是对儿童脾脏免疫功能的保留,脾脏切除术后暴发性感染的预防,其意义不容忽视或低估。
改良的脾-肺固定术,省去腹部切口,减少了创伤,缩短了手术时间;附加了大网膜与肺的固定,使门肺间的侧支形成更快、更多;又由于大网膜的固有特性,如粘连、游走、包裹、填塞作用,对止血、炎症局限和防治膈疝等,均有积极意义。切脾、断流术后,常有不明原因的高热,而在脾-肺固定术后则少见。尽管在随访的病例中少数出现杵状指,但无其他相伴症状。除患有肺部疾病或伴有大量腹水者外,脾-肺固定术可适合于各种类型的门脉高压症。
肠-腔C形人工血管架桥的优点:
(1)人工血管与自体血管之间的交角小于45°,符合血流动力学要求,而H形架桥易产生涡流,易发生血栓。
(2)门静脉血栓形成后,门静脉血液入肝受阻,肠-腔分流可同时降低系膜区和脾胃区的压力,附加脾动脉结扎和脾部分切除、冠状静脉结扎,对防治消化道出血、脾肿大和脾功能亢进,均有缓解作用。
(3)对脾脏已切除的再发出血的病例,肠-腔分流术应属最佳选择。
(4)带支架环的人工血管,分流口径固定,有控制分流量的作用,此优于肠-腔侧侧分流。
(5)肠-腔C形架桥术,因脾脏的免疫、滤过等生理功能得以维持,术后再发病例,尚可再做脾-肺固定术以建立门肺分流来补救。



 流行病学
流行病学
 病因
病因
 发病机制
发病机制
 临床表现
临床表现
 并发症
并发症
 实验室检查
实验室检查
 其他辅助检查
其他辅助检查
 诊断
诊断
 鉴别诊断
鉴别诊断
 治疗
治疗
 预防
预防